原文发表在Journal of Antibody-drug Conjugates, 作者:Nigel Herbert, Repligen CTech; Joshua Das和Prlya Patel, Analytical Research and Development, Global NBE Analytical R&D, AbbVie.
抗体-药物偶联物 (ADC) 是设计用于靶向和杀死肿瘤细胞的复杂分子。ADC 由单克隆抗体、药物接头和药物(有效负载)组成,其中抗体通常靶向肿瘤细胞上的蛋白质。UV-Vis 光谱 光程 solovpe 样品
简介
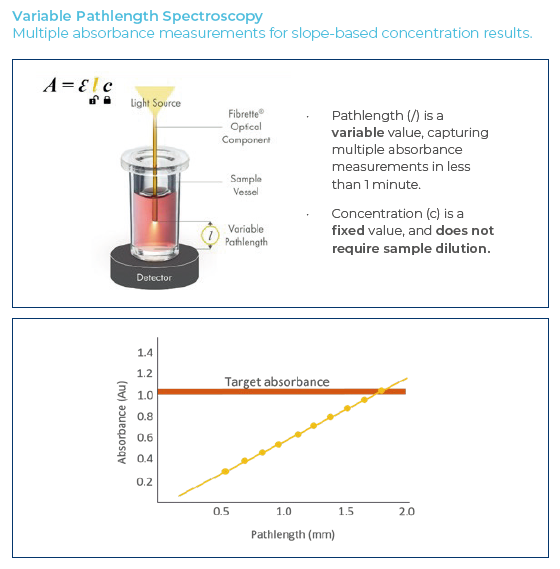
ADC 是由与具有生物活性的细胞毒性有效载荷连接的抗体组成的复杂分子。ADC 是一类新型高效生物药物,因为它们结合了单克隆抗体的靶向能力和细胞毒药物的抗癌能力。抗体与癌细胞表面的特定蛋白质结合,使 ADC 被内化在细胞内,其中接头被降解,细胞毒性有效载荷被释放。因为这些药剂可以直接向肿瘤细胞传递高细胞毒性的有效载荷,它们可用于实现对目标癌细胞的高杀伤力,同时使健康细胞不受伤害。确定 ADC 的蛋白质浓度有助于评估分子的功效。 UV-Vis 光谱法是确定 ADC 蛋白质浓度的常用分析方法。通过利用比尔-朗伯定律,分光光度计可以识别样品的浓度。Beer-Lambert 定律指出溶液的吸光度与该溶液的浓度成正比。吸光度和浓度之间的关系可以表示为 A = ε*l*c 其中 A 是测量的吸光度,ε 是摩尔吸光系数,l 是光程,c 是样品的浓度。尽管传统的分光光度计是常用的方法之一,但这种应用可能会带来挑战。首先,传统分光光度计使用的固定 1 cm 光程限制了仪器的线性范围。在大多数情况下,需要对样品进行连续稀释以确保测定在仪器的线性范围内。这可能导致高达 30% 的错误,从而质疑测量的有效性。此外,有效载荷的存在可能会干扰测量。如果未正确识别有效载荷和抗体的发色团,可能会导致蛋白质浓度高估。 SoloVPE 是一种新兴的UV-Vis 技术,它通过利用斜率 。 为了启用斜率光谱方程,将路径长度项 l 移动到方程的左侧,其中 A/l = ε*c 。 A/l 项是每次光程变化时吸光度的变化,也称为方程的斜率 m 。 这种替换导致斜率光谱方程可以表示为 m = ε*c 。 斜率是方程中关键的值,因为它允许我们确定样品浓度或摩尔吸收系数。
SoloVPE 通过测量 Fibrette 光纤棒底部和样品容器底部之间的距离来定义其光程范围。 SoloVPE 的集成硬件和软件允许系统将 Fibrette 光纤棒从 5 μm 上下移动到 15 mm,光程分辨率为 5 μm 步长(图 1)。 测量的线性回归系数 (R2) 证实了与比尔定律的相关性。 SoloVPE 要求所有测量的 R2 ≥ 0.999 才被视为有效。 通过证明吸光度值与光程值成比例变化,接近 1 的值证实了与比尔定律的强相关性。 因此,SoloVPE 可以测量宽范围的浓度,而无需大量的样品制备和稀释。 SoloVPE 的可变光程技术、快速分析速度和增强的光谱范围使其能够产生准确、线性和可重复的结果。
材料和方法
材料
Abbvie
• ADC 1 Multi-wavelength [货号:ABBV-400]
• 离心过滤装置 Ultra-2mL Ultracel 3K [货号:B9AA89322]
• HPCE Water [货号:BCCF5932]
CTech
• SoloVPE [货号:SYS-VPE-SOLO5]
• Cary 60 紫外-可见分光光度计 [货号:IN-CARY 60 或 Agilent货号: G6860A]
方法
ADC 由 anti-PRLR/anti-EGFR 单克隆抗体组成,该抗体通过马来酰亚胺己酰-缬氨酸-丙氨酸接头与吡咯并苯二氮卓 (PBD) 偶联。PBD 在 280 nm 处有显着吸收,因此 ADC 的吸光度取决于蛋白质和 PBD 含量。PBD 在 370 nm 处具有更大的UV λ,而单克隆抗体仅在 280 nm 处有吸收。因此,为了确定蛋白质浓度,需要读取 280 nm 和 370 nm 的吸光度读数,并且必须应用 0.2 的校正因子来计算 PBD 在280 nm 的吸光度。下面的等式说明了如何确定蛋白质浓度。
蛋白质浓度 (mg/ml) = (M280-(M370*CF)) / ε *10
其中:
M280 = 280 nm 处的斜率。
M370 = 370 nm 处的斜率。
CF = 校正因子。
ABBV-400 的 CF 为 0.2。
ε = 消光系数,即 1.37 (mg/ml)cm-1。
在不同浓度(高蛋白含量,120%、100%、80%、50% 和 20%)下对 ADC 进行三次测量。通过使用离心过滤装置将标称样品 (100%, 22.5 mg/ml) 浓缩至更高的蛋白质浓度来配制高蛋白质含量。将材料以 4000 RPM 离心 8 分钟以达到 30.8 mg/ml 的最终浓度。然后将该材料稀释至 120% (27 mg/ml) 和 80% (18 mg/ml),这是大多数验证实验的工作浓度。将样品进一步稀释至 50% (11.25 mg/ml) 和 20% (4.5 mg/ml) 以评估线性度。使用了小型塑料比色皿,只需要 120 ul 的样品体积。根据每个验证研究中提供的接受标准收集和评估数据。
结果
精度(可重复性)
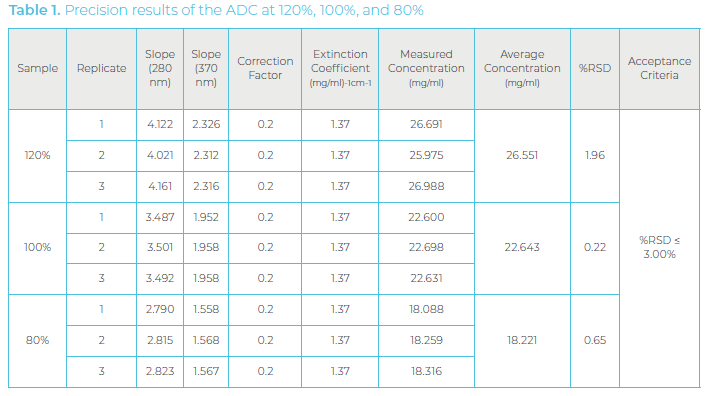
通过在标称浓度的 120%、100% 和 80% 下测量 ADC 来评估精度。每个目标浓度一式三份测量。本研究要求每个浓度的 %RSD ≤3.00%。如表 1 所示,所有浓度水平的三次读数均远低于3.00%。最高 %RSD 为 1.96%,这是 120% 样品的结果。纯样品 (100%) 在三次测量之间表现出更佳精度。精密度研究结果表明该方法是精密的。
准确性
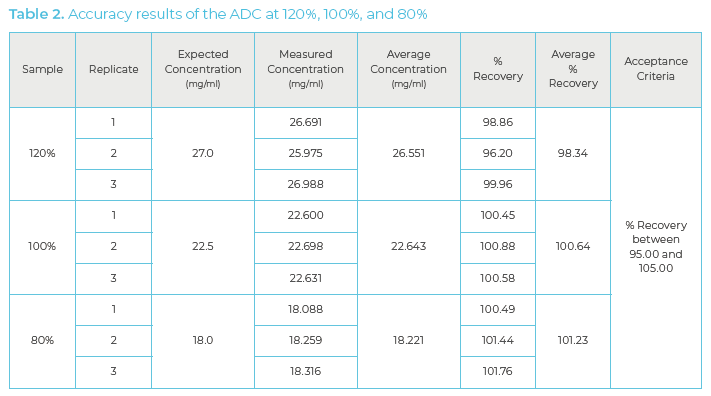
通过计算在精密度研究中测量的不同浓度水平的 % 回收率来评估准确度。本研究要求测量浓度在目标浓度的 95% 至 105% 范围内。下面的等式说明了如何计算回收率百分比。纯样品的测量浓度与预期浓度显示出近乎完美的相关性,平均回收率为 100.636。如表 2 所示,所有测得的浓度均在研究的可接受标准范围内。
% 回收率 = (测量浓度) / (目标浓度) * 100
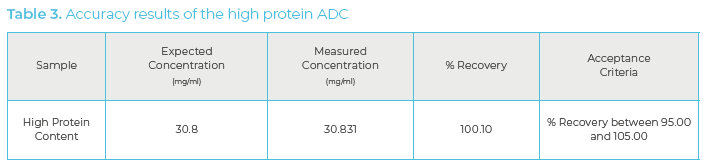
还分析了高蛋白样品以评估该方法的准确性。与纯样品的 % 回收率相似,高蛋白样品的测量浓度与预期浓度显示出近乎完美的相关性,回收率为 100.10(表 3)。
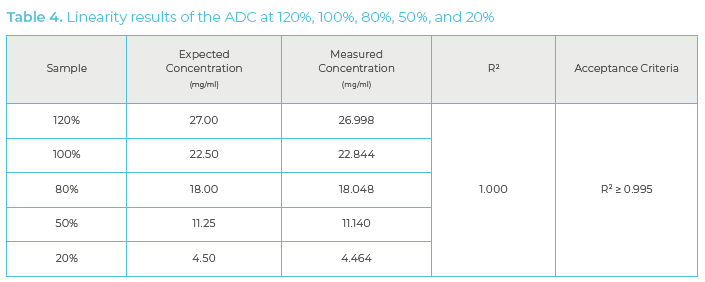
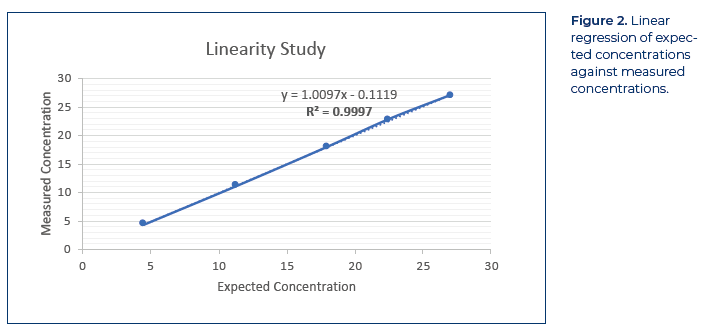
线性度
通过评估 ADC 在 120%、100%、80%、50% 和 20% 时的线性回归来评估线性度。将每个水平的预期浓度与测量浓度进行比较(表 4),研究要求 R2 ≥ 0.995。结果中的 R2 为 1.000,表明预期浓度和测量浓度之间存在很大的线性相关性。图 2 说明了浓度组之间的线性一致性。线性回归分析结果表明该方法是线性的。
讨论
精度是该方法评估的第一项研究。所有三次测量都显示出非常一致的结果,导致 %RSD 低于 3%。120% 样品的高 %RSD为 1.96%,仍远低于验收标准。120% 样品的 3 个重复 2 的变异更 大,对%RSD 的影响更大。这很可能是由于样品的同质性。很可能需要额外的混合,这会导致更严格的 %RSD。标称样品的精密度更高,%RSD 为 0.22%。由于没有稀释或样品处理,因此纯样品有望具有精度。 准确性是下一个要评估的研究。本研究通过确保 120%、100%、80% 和高蛋白样品的回收率百分比在 95% 和 105% 范围内进行评估。所有测量均通过了验收标准,纯净且高蛋白的样品显示出最佳准确性。纯样品的平均回收率为 100.64%,高蛋白样品的回收率为 100.10%,表明测量浓度与预期浓度之间的比较接近完美。与精密度研究类似,120% 样品与目标的变异性更 高,平均回收率为98.34%。同样,这是由于重复 2 的变异更大,回收率为96.20%,这很可能可以通过额外的样品混合来弥补。 线性是要评估的最后一项研究。本研究的验收标准要求 R2 ≥0.995。观察到的 R2 为 1.000,表明稀释系列的测量浓度与预期浓度具有很大的线性一致性。SoloVPE 还评估每次测量的线性度,确保每次分析的斜率 R2 ≥ 0.999。这很关键,因为如果他们的测量结果与比尔定律线性一致,它会给用户带来有效性。 除了分析蛋白质浓度,药物抗体比 (DAR) 是 ADC 的一个重要属性。DAR 是与抗体偶联的药物的平均数量,可以帮助确定药物的功效。DAR 是通过将有效负载浓度除以抗体浓度来计算的。尽管本研究未评估 DAR,但 SoloVPE 可用于准确计算该函数。 要计算 DAR,必须确定有效载荷浓度和抗体浓度。如果药物的校正因子未知,则可以使用线性代数方程来确定这两种浓度。可以使用以下等式确定药物的浓度:
Cdrug = ((M280 * εmAbλ(D) - Mλ(D) * εmAb280)/ (εdrug280 * εmAb λ(D) - εdrug λ(D) * εmAb280)) * 10
CmAb = ((M280 * εdrugλ(D) - Mλ(D) * εdrug280)/ (εmAb280 * εdrug λ(D) – εmAb λ(D) * εdrug280)) * 10
DAR = Cdrug/CmAb
如上所示,需要额外的药物消光系数来评估有效载荷浓度,而有效载荷浓度又将用于计算 DAR。SoloVPE 软件的 Multi-Q 功能允许用户同时在多个波长上进行浓度测量。此外,系统的用户结果功能允许用户同时计算上述所有方程。这些特性使 SoloVPE 成为量化 DAR 的理想选择。对于这项研究,需要进一步分析来证明 SoloVPE 有效计算 DAR 的能力。 高精度、一致的可重复性和宽线性范围使 SoloVPE 是 ADC 整个生命周期中蛋白质含量测定的合适选择。 样本可用性,特别是在早期研究期间,可能非常有限; 因此,SoloVPE 使用少量样品测量蛋白质含量的能力是优于传统 UV-Vis 系统的优势。 此外,与传统的 UV-Vis 方法相比,运行 SoloVPE 所需的样品制备要省力得多,传统的 UV-Vis 方法通常必须先将样品先用兼容的无干扰稀释剂稀释到线性范围内。 在SoloVPE 的情况下,可以使用标称浓度直接测量样品,从而减少方法开发和样品制备所需的时间,从而可以根据蛋白质含量快速做出关键决策。 总之,SoloVPE 是量化ADC 蛋白质浓度的首选方法。斜率光谱法允许 SoloVPE 克服传统分光光度计常见的问题。可变光程技术能够量化高浓度样品,而无需稀释和繁重的样品制备。此外,该软件允许系统配置多个计算,这是量化 ADC 的理想选择。每个验证研究中的所有验收标准均通过,证明该方法是精确、准确和线性的。SoloVPE 已被证明是支持量化 ADC 蛋白质浓度的可靠分析方法。